
Une chambre de test de stabilité des médicaments, également connue sous le nom de chambre de test de stabilité ou chambre environnementale, est un équipement spécialisé utilisé dans l'industrie pharmaceutique pour évaluer la stabilité des médicaments, des vaccins et d'autres produits de santé dans diverses conditions environnementales.
Modèle : TG-250SD
Capacité : 250L
Étagère : 3 pièces
Couleur : Blanc cassé
Dimension intérieure : 600×500×830 mm
Dimension extérieure : 740×890×1680 mm
Description
Une chambre de test de stabilité des médicaments est conçue pour maintenir des conditions spécifiques de température, d'humidité et d'éclairage, qui peuvent simuler diverses conditions environnementales auxquelles le médicament peut être exposé pendant le stockage et le transport. Le but des tests de stabilité des médicaments est de garantir que le médicament conserve sa qualité, sa sécurité et son efficacité pendant sa durée de conservation et qu'il répond aux exigences réglementaires d'approbation.
spécification
|
Modèle |
TG-80SD |
TG-150SD |
TG-250SD |
TG-500SD |
TG-800SD |
TG-1000SD |
|
Dimensions intérieures |
400×400×500 |
550×405×670 |
600×500×830 |
670×725×1020 |
800×590×1650 |
1050×590×1650 |
|
Dimension extérieure |
550×790×1080 |
690×805×1530 |
740×890×1680 |
850×1100×1930 |
1360×890×2000 |
1610×890×2000 |
|
Capacité |
80L |
150L |
250L |
500L |
800L |
1000L |
|
Écart de température |
0°C~65°C |
|||||
|
Fluctuation de température : ±0,5 °C ; Uniformité de la température : ±2,0 °C |
||||||
|
Plage d'humidité |
35 % ~ 95 % d'humidité relative |
|||||
|
Écart d'humidité |
±3,0 % H.R. |
|||||
|
Éclairage |
N / A |
|||||
|
Contrôle de la température |
Méthode de réglage de la température équilibrée |
|||||
|
Contrôle de l'humidité |
Méthode de réglage de l'humidité équilibrée |
|||||
|
Réfrigération |
Deux ensembles de compresseurs hermétiques importés d'origine indépendants commutent automatiquement (LHH-80SD : un ensemble) |
|||||
|
Matériau intérieur |
Acier inoxydable brossé anticorrosion SUS#304 |
|||||
|
Matériau extérieur |
Tôle d'acier laminée à froid avec pulvérisation de poudre électrostatique |
|||||
|
Isolation |
Laine de fibre de verre superfine / polyuréthane |
|||||
|
Manette |
Contrôleur LCD programmable |
|||||
|
Capteur |
Résistance platine PT100 / Capteur d'humidité capacitif |
|||||
|
Étagères |
2 pièces |
3 PIÈCES |
3 PIÈCES |
4 PIÈCES |
||
|
Consommation d'énergie |
2000W |
2100W |
2300W |
3750W |
7150W |
7150W |
|
Source de courant |
220 V/50 Hz |
380 V/50 Hz |
||||
|
Insérer une mini-imprimante |
1 jeu |
|||||
|
Dispositifs de protection |
Protection contre la surchauffe du compresseur, protection contre la surchauffe du ventilateur, protection contre la surchauffe, protection contre la surpression du compresseur, protection contre les surcharges, protection contre le manque d'eau. |
|||||
|
Condition de travail |
+5~30℃ |
|||||
Protection de sécurité:
· Limiteur de température indépendant : un arrêt indépendant et une alarme à des fins de protection thermique pendant le test.
·Système de réfrigération : protection contre la surchauffe, la surintensité et la surpression du compresseur.
·Chambre d'essai : protection contre la surchauffe, surchauffe du ventilateur et du moteur, défaillance/inversion de phase, synchronisation de l'ensemble de l'équipement.
·Autres : protection contre les fuites et les pannes, protection par fusible contre les surcharges, alarme de signal audio, protection contre les fuites de courant et surcharge
Protection.
Courbe de température et d'humidité :
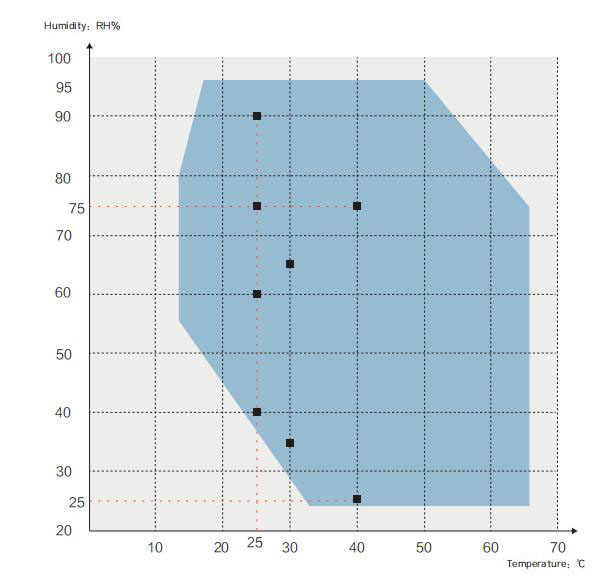
■Directives pharmacopées sur la stabilité des médicaments bruts et des préparations ainsi que les
conditions d’essai de température et d’humidité requises dans les directives ICH :
La température ambiante pour les tests suivants doit être comprise entre 15 et 25 ℃
√Test accéléré : 40 ℃ ± 2 ℃ / 75 % ± 5 % HR, ou 30 ℃ ± 2 ℃ / 65 % ± 5 % HR
√Test d'humidité élevée : 25 ℃ / 90 % ± 5 % RH, ou 25 ℃ / 75 % ± 5 % RH
√Test à long terme : 25 ℃ ± 2 ℃ / 60 % ± 5 % HR, ou 30 ℃ ± 2 ℃ / 65 % ± 5 % HR
√Pour les tests accélérés des préparations médicamenteuses conditionnées dans des emballages semi-perméables
contenants, tels que des poches de perfusion préparées par LDB, des ampoules en plastique et des oculaires
récipients de préparation, etc., les tests doivent être effectués à une température de 40 ℃ ± 2 ℃/25 % ± 5 % RH
√Pour les tests à long terme des préparations pharmaceutiques conditionnées en semi-
récipients perméables, il doit être à une température de 25℃±2℃/40%±5%RH ou 30℃±2℃/35%±5%RH
Caractéristique de la chambre d'essai de stabilité des médicaments
La chambre de test de stabilité des médicaments est disponible en différentes conceptions et modèles, mais elle présente généralement les caractéristiques suivantes :
1.Contrôle de la température : La chambre de test de stabilité des médicaments maintient un contrôle précis de la température, la plage de température peut être aussi basse que -20 °C jusqu'à 70 °C.
contrôle 2.Humidity : Le niveau d'humidité à l'intérieur de la chambre d'essai de stabilité de médicament peut être ajusté pour simuler l'humidité différente. Ceci est particulièrement important pour les médicaments sensibles à l’humidité, tels que certains types de formes posologiques solides et de produits biologiques.
• Contrôleur à écran tactile programmable
. 100 programmes, 1000 segments 999 étapes, 99 heures 59 minutes pour chaque segment.
. Fonction de calcul automatique P.I.D.
. Interface de communication RS485/une imprimante intégrée disponible, pour le stockage des données et la lecture de la courbe historique.
. Enregistrement des données et affichage du diagnostic de défaut, une fois qu'un défaut se produit, la cause du défaut sera affichée dynamiquement sur le contrôleur.

3.Contrôle de l’éclairage : Certains médicaments sont sensibles à la lumière et peuvent se dégrader s’ils sont exposés à certaines longueurs d’onde de lumière. Par conséquent, la chambre d'essai de stabilité des médicaments Climatest Symor® dispose de commandes d'éclairage, comme la lumière UV, pour déterminer l'effet de la lumière sur le produit médicamenteux.
Contrôle 4.Airflow : La chambre d'essai de stabilité des médicaments dispose de systèmes de circulation d'air pour maintenir une température et une humidité constantes et uniformes dans toute la chambre.
5. Enregistrement et surveillance des données : la chambre de test de stabilité des médicaments est équipée de capteurs et de systèmes d'enregistrement de données qui surveillent et enregistrent la température, l'humidité et d'autres paramètres environnementaux, qui peuvent être utilisés pour générer des rapports et valider la stabilité du produit.
Dans l'ensemble, la chambre de test de stabilité des médicaments vise à garantir que les médicaments sont stockés et testés dans des conditions environnementales contrôlées qui simulent des conditions réelles, et à fournir des données de stabilité précises et fiables pour l'approbation réglementaire.
Zone de test :
La zone de test d'une chambre de test de stabilité des médicaments est en acier inoxydable SUS304 et est conçue pour simuler des conditions constantes de température, d'humidité et d'éclairage. La chambre est équipée de capteurs de température et d'humidité de haute précision pour surveiller et maintenir ces conditions climatiques.
Il existe des racks ou des étagères pour contenir les échantillons de médicaments, ces étagères sont réglables en hauteur et les échantillons sont généralement placés dans des flacons ou des conteneurs en verre hermétiquement fermés pour éviter toute contamination.

Avantages de la chambre d'essai de stabilité des médicaments
Alors, quels avantages la chambre d’essai de stabilité pharmaceutique Climatest Symor® peut-elle vous apporter ?
. Contrôle qualité : la chambre de test de stabilité pharmaceutique aide les entreprises pharmaceutiques à tester la qualité et la sécurité de leurs produits en fournissant des données sur les performances des médicaments au fil du temps. Ces données aident les fabricants à prendre des décisions éclairées concernant la durée de conservation, le stockage et l'emballage de leurs produits.
. Conformité réglementaire : la chambre de test de stabilité des médicaments est requise par les agences de réglementation, telles que la FDA, pour tester la stabilité des médicaments et autres produits de santé.
. Réduire les coûts : en testant la stabilité des médicaments avant leur mise sur le marché, les sociétés pharmaceutiques peuvent réduire le risque de pannes et de rappels de produits. Cela peut entraîner des économies significatives.
. Développement de produits amélioré : en testant la stabilité du médicament dans diverses conditions environnementales, les fabricants peuvent identifier les problèmes potentiels dès le début du processus de développement.
Dans l’ensemble, la chambre de test de stabilité des médicaments joue un rôle essentiel pour garantir la sécurité, l’efficacité et la qualité des médicaments et autres produits de santé.
La fonction de la chambre d'essai de stabilité des médicaments
La chambre de test de stabilité des médicaments est conçue pour répondre aux exigences réglementaires strictes et aux normes industrielles, telles que celles fixées par la Conférence internationale sur l'harmonisation (ligne directrice ICH). Les chambres peuvent être utilisées à diverses fins, notamment :
*Tests de stabilité au stockage à long terme : ce type de test est utilisé pour déterminer la stabilité d’un médicament sur une période prolongée, généralement plusieurs années.
* Tests de durée de conservation : les chambres de stabilité en produits pharmaceutiques sont utilisées pour déterminer la durée de conservation d'un médicament, c'est-à-dire la durée pendant laquelle un produit peut être stocké dans des conditions spécifiques sans perdre sa puissance, son efficacité ou sa qualité.
*Tests de stabilité accélérés : ce type de test est utilisé pour évaluer la stabilité d'un médicament dans des conditions extrêmes, telles que des températures et une humidité élevées, dans un court laps de temps.
Sur la base des résultats des tests de stabilité, le fabricant peut déterminer la durée de conservation du produit et apporter les ajustements nécessaires à la formulation ou à l'emballage pour garantir que le produit reste stable dans le temps. Ces informations sont essentielles aux organismes de réglementation, qui les utilisent pour déterminer les exigences appropriées en matière de stockage et de manipulation du médicament.
Dans l’ensemble, la chambre de test de stabilité des médicaments joue un rôle essentiel pour garantir la sécurité et l’efficacité des médicaments et constitue un outil essentiel pour l’industrie pharmaceutique.

Test de facteurs d'influence dans une chambre de stabilité des médicaments
La chambre de test de stabilité des médicaments est souvent utilisée dans les installations de recherche et développement pharmaceutique, de contrôle qualité et de fabrication, ainsi que dans les agences de réglementation qui supervisent l'approbation et la sécurité des médicaments.
Le test des facteurs d'influence (test de stress, également connu sous le nom de test intensif) vise à explorer la stabilité inhérente du médicament, à comprendre les facteurs qui affectent sa stabilité et les voies de dégradation possibles. Fournir une base scientifique pour le processus de production des préparations, l'emballage, les conditions de stockage et l'établissement de méthodes d'analyse des produits de dégradation.
Vous trouverez ci-dessous un cas de test pour montrer le facteur d'influence testé sur les matières premières pharmaceutiques :
①Test à haute température :
Température : @60°C
Temps : 10 jours
Prélever des échantillons le 5èmejour et testez-les selon les éléments clés de l'inspection de stabilité. Si la teneur des échantillons est inférieure à la limite spécifiée, effectuez le test ci-dessus à 40 °C ; si pas de changement significatif à 60°C, inutile de réaliser le test à 40°C.
②Test d'humidité élevée :
Température : @25°C
Humidité relative : 90 % ± 5 %
Temps : 10 jours
Prélever des échantillons le 5èmejour et 10èmeJour et testez-les en fonction des éléments clés de l'inspection de stabilité. pendant ce temps, pesez avec précision le poids des échantillons avant et après le test, pour étudier les performances d'absorption d'humidité et de déliquescence.
Si le gain de poids est >5 %, l'essai ci-dessus doit être effectué selon la même méthode sous une humidité relative de 75 % ± 5 % ;
Si le gain de poids est <5 % et que d'autres conditions répondent aux exigences, l'essai à 75 % ± 5 % ne doit pas être effectué.
③Test d'irradiation lumineuse intense :
Éclairage : 4500LX ± 500LX
Durée : 10 jours
Prélever des échantillons le 5èmejour et 10èmeJour et testez-les en fonction des éléments clés d'inspection de stabilité, veuillez faire attention aux changements d'apparence des échantillons.
Certificats de chambre d'essai de stabilité des médicaments
Les certificats de la chambre de test de stabilité des médicaments sont des documents officiels délivrés par les fabricants ou des organismes tiers accrédités. Ils vérifient les performances et la conformité de la chambre aux réglementations et normes en vigueur. Climatest Symor® est certifié ISO9001:2015, toutes les chambres d'essai de stabilité sont approuvées CE.

Photos d'installation sur site
L'installation de chambres de test de stabilité des médicaments nécessite une planification minutieuse et une attention aux détails pour garantir qu'elles sont correctement installées et fonctionnent comme prévu. Les photos suivantes sont prises sur le site de l'utilisateur final.
